Traduction de l’étude
 SOUTIEN À LA NUTRITION AU TEMPS DE COVID-19
SOUTIEN À LA NUTRITION AU TEMPS DE COVID-19Alessandro Laviano Nutrition Disponible en ligne le 2 avril 2020, 110834
La nutrition est un déterminant clé de la santé [1]. Plus important encore, la nutrition fait partie du traitement des maladies aiguës et chroniques. Cela s'applique en particulier aux affections pour lesquelles un traitement étiologique n'a pas encore été découvert et validé. L'épidémie de virus Ebola de 2014-2016 en Afrique de l'Ouest a démontré que les soins de soutien immédiats réduisent considérablement les taux de létalité [2,3]. Cela pourrait bien s'appliquer à la pandémie actuelle de SRAS-CoV-2 qui ravage le monde.
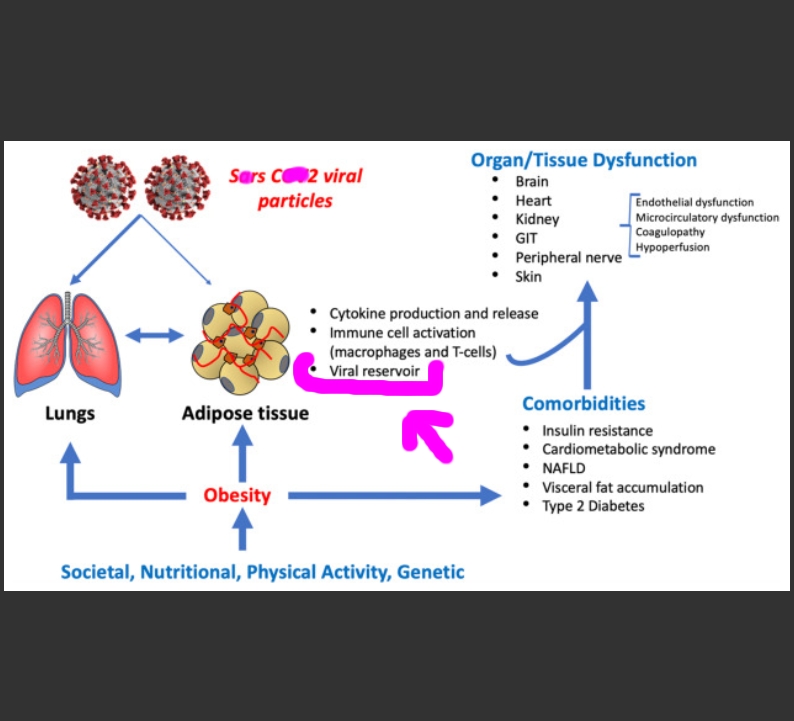
De nouvelles preuves montrent que COVID-19 est associé à des résultats négatifs chez les patients âgés, comorbides et hypoalbuminémiques [4]. Ces caractéristiques ne sont pas spécifiques à la population chinoise puisqu'elles ont également été rapportées chez des patients nord-américains COVID-19 [5]. Lorsqu'elles sont considérées ensemble, la littérature émergente sur les patients COVID-19 met indirectement en évidence la pertinence de la nutrition pour déterminer éventuellement leurs résultats. L'âge avancé et la présence de conditions comorbides sont presque toujours associés à une altération de l'état nutritionnel et à la sarcopénie, indépendamment de l'indice de masse corporelle (IMC) [6]. Fait intéressant, un IMC élevé semble être lié à un mauvais pronostic chez les patients comorbides COVID-19, ce qui indique en outre un rôle possible de l'obésité sarcopénique dans l'influence sur les résultats [7]. De plus, la lymphopénie, marqueur de la malnutrition, est un facteur pronostique négatif chez les patients COVID-19 [4]. Il est reconnu que les taux de circulation d'albumine ne doivent pas être considérés comme un marqueur nutritionnel chez les patients présentant une réponse inflammatoire, mais le récent rapport selon lequel une faible préalbumine prédit la progression vers le syndrome de détresse respiratoire aiguë (SDRA) [8] suggère qu'un faible apport nutritionnel contribue au résultat. . Enfin, le moment de l'intervention nutritionnelle semble être critique, car la plupart des patients évoluent rapidement de la toux à la dyspnée, puis à l'insuffisance respiratoire et à l'admission en unité de soins intensifs pour la ventilation mécanique [4,5].
L'état nutritionnel semble être un facteur pertinent influençant les résultats des patients atteints de COVID-19, mais peu d'informations ont été publiées jusqu'à présent sur l'impact du soutien nutritionnel précoce chez les patients pré-USI et les patients gravement malades atteints de COVID-19. La Commission nationale de la santé de la République populaire de Chine et l'Administration nationale de la médecine traditionnelle chinoise recommandent la mise en œuvre de «soins de soutien renforcés pour assurer un apport énergétique suffisant» [9]. Zhang & Liu a récemment élaboré une liste de nutriments susceptibles d'avoir des effets anti-coronavirus, sur la base d'études in vitro et cliniques [10]. Cependant, aucune des publications disponibles n'a jusqu'à présent discuté de la manière d'adapter les directives actuellement disponibles pour la thérapie nutritionnelle pendant la maladie au scénario clinique spécifique de COVID-19. Un protocole basé sur l'expérience clinique tirée des défis quotidiens posés par les patients COVID-19 peut aider à stimuler la discussion concernant les options de nutrition-livraison, conduisant à son tour à des améliorations dans la standardisation des approches nutritionnelles et l'identification des soins optimaux
utrition publie ci-joint un protocole pragmatique pour la prestation d'une thérapie nutritionnelle chez les patients pré-ICU avec COVID-19. Le protocole a été conçu par une équipe multidisciplinaire d'experts travaillant en Lombardie, centre de la crise italienne du COVID-19 [11]. Dans le protocole, certaines procédures diffèrent des directives nutritionnelles disponibles. Cependant, les écarts semblent justifiés par les caractéristiques cliniques spécifiques des patients COVID-19. De plus, l'environnement hospitalier (c.-à-d. Pénurie de médecins et d'infirmières, augmentation de la charge de travail quotidienne, nécessité de réduire le contact avec les patients infectés par le SRAS-CoV-2, un pathogène hautement infectieux) a influencé la décision de préférer certaines voies d'alimentation en contradiction apparente avec directives internationales. Par conséquent, le protocole ne doit pas être considéré comme une ligne directrice mais plutôt comme un exemple de la stratégie mise en œuvre par une équipe d'experts pour fournir des soins nutritionnels aux patients à haut risque de malnutrition dans un environnement de travail difficile. Chez Nutrition, nous espérons que ce protocole suscitera un débat et éventuellement de nouvelles propositions pour relever les défis cliniques et organisationnels de COVID-19. La nutrition est prête à servir de tribune pour l'amélioration progressive des soins nutritionnels de ces patients.
Il est reconnu que le protocole ne traite pas la question importante de son efficacité. Cela semble pertinent, car l'inflammation de base limite l'impact du soutien nutritionnel sur les résultats cliniques [12]. Étant donné que les patients COVID-19 présentent une réponse inflammatoire accrue lors de leur admission à l'hôpital [4], le protocole peut nécessiter des ajustements pour cibler également l'inflammation. En outre, la question du contrôle de la glycémie des patients diabétiques COVID-19 peut nécessiter un examen plus approfondi [13]. Enfin, il est reconnu que ce protocole ne traite pas des soins nutritionnels des patients COVID-19 gravement malades. Il s'agit d'un point clinique crucial, car une fois que le patient doit être intubé et ventilé mécaniquement, le séjour en soins intensifs peut être prolongé [4]. L'European Society of Intensive Care Medicine et la Society of Critical Care Medicine viennent de publier des lignes directrices pour la prise en charge des patients gravement malades COVID-19 qui ne répondent pas aux besoins non satisfaits de soins nutritionnels [14]. En attendant des recommandations spécifiques sur la prise en charge nutritionnelle des patients COVID-19 en USI, les lignes directrices actuellement disponibles sur la nutrition clinique chez les patients en USI sont susceptibles de répondre aux besoins des patients COVID-19. Cependant, il reste à prouver si les besoins nutritionnels et métaboliques des patients sous COVID-19 ventilés sont similaires à ceux des patients atteints de SDRA. Selon les récentes directives ESPEN, la nutrition entérale est préférée chez les patients en USI recevant une ventilation mécanique [15]. Cependant, les besoins spécifiques des patients atteints de COVID-19 peuvent nécessiter l'adoption d'une ventilation sujette et / ou d'un blocage neuromusculaire [5,14]. Bien que la nutrition entérale en position couchée se soit avérée faisable et sûre [16], sa mise en œuvre dans la pratique quotidienne pourrait être difficile. Cette question peut être particulièrement pertinente pour les jeunes professionnels sans expertise spécifique en nutrition clinique, appelés à agir et à prendre des décisions dans un environnement difficile et jusqu'à présent sans indications et protocoles spécifiques. De plus, l'hypoxémie potentiellement mortelle nécessite un retard de la nutrition entérale [15]. De plus, les symptômes gastro-intestinaux, notamment les vomissements et la diarrhée, sont fréquents chez les patients COVID-19 [17]. Chez les patients atteints de SDRA / lésion pulmonaire aiguë, les régimes entériques contenant de l'acide eicosapentaénoïque, de l'acide gamma-linolénique et des antioxydants peuvent offrir un avantage clinique en oxygénation et en jours de ventilation [15], mais la possibilité que la pneumonie liée au SRAS-CoV-2 puisse répondre à une entérale spécifique les régimes restent à déterminer. Une autre question encore sans réponse concernant les soins nutritionnels des patients gravement malades atteints de COVID-19 est de savoir si la modulation de la réponse inflammatoire par des émulsions lipidiques spécifiques pourrait offrir un avantage supplémentaire par rapport aux corticostéroïdes et aux médicaments anti-IL-6. Enfin, la dysphagie acquise après ventilation et la faiblesse acquise en unité de soins intensifs posent d'énormes défis à la réadaptation réussie des survivants du COVID-19 et doivent être abordées tôt et de manière globale pendant la période de récupération. Les sociétés scientifiques internationales de nutrition, y compris la Société européenne pour la nutrition clinique et le métabolisme - ESPEN, relèvent le défi d'élaborer des lignes directrices mises à jour qui sont spécifiques aux besoins des patients COVID-19 gravement malades, et leurs efforts seront disponibles dans les prochains journées.
SARS-CoV-2 est là pour rester. Elle ravagera des pays et des continents, disparaîtra puis réapparaîtra ici et là, lorsque les conditions environnementales et sociales le permettront. Il vaut mieux être préparé.
Traduction de l’étude
 Interventions potentielles pour un nouveau coronavirus en Chine: une revue systématique
Interventions potentielles pour un nouveau coronavirus en Chine: une revue systématiqueLei Zhang Yunhui Liu J Med Virol 13 février 2020
Une flambée d'une nouvelle infection à coronavirus (COVID ‐ 19 ou 2019 ‐ CoV) a fait peser des menaces importantes sur la santé et l'économie internationales. En l'absence de traitement pour ce virus, il est urgent de trouver des méthodes alternatives pour contrôler la propagation de la maladie. Ici, nous avons effectué une recherche en ligne pour toutes les options de traitement liées aux infections à coronavirus ainsi qu'à certaines infections à virus ARN et nous avons constaté que les traitements généraux, les traitements spécifiques aux coronavirus et les traitements antiviraux devraient être utiles dans la lutte contre le COVID ‐ 19. Nous suggérons que l'état nutritionnel de chaque patient infecté soit évalué avant l'administration de traitements généraux et que les vaccins ARN-virus pour enfants actuels, y compris le vaccin antigrippal, soient immunisés pour les personnes non infectées et les agents de santé. De plus, du plasma convalescent doit être administré aux patients COVID ‐ 19 s'il est disponible. En conclusion, nous suggérons que toutes les interventions potentielles soient mises en œuvre pour contrôler le COVID ‐ 19 émergent si l'infection est incontrôlable.
1. INTRODUCTION
Les coronavirus (CoV) appartiennent à la sous-famille des Orthocoronavirinae de la famille des Coronaviridae dans l'ordre des Nidovirales, et cette sous-famille comprend les α ‐ coronavirus, β ‐ coronavirus, γ ‐ coronavirus et delta ‐ coronavirus.1 Les coronavirus provoquent principalement des infections enzootiques chez les oiseaux. et, au cours des dernières décennies, se sont également révélées capables d'infecter les humains.2 L'épidémie de syndrome respiratoire aigu sévère (SRAS) en 2002 et le syndrome respiratoire du Moyen-Orient (MERS) en 2012 ont démontré la létalité des coronavirus lorsqu'ils traversent la barrière des espèces et infectent les humains.2 Le SRAS ‐ CoV et le MERS ‐ CoV appartiennent tous à la famille des β ‐ coronavirus.3 Récemment, un nouveau coronavirus pseudo-grippal (COVID ‐ 19) lié aux coronavirus MERS et SRAS a été trouvé à la fin de 2019 en Chine4, 5 et la preuve de la transmission interhumaine a été confirmée parmi les contacts étroits.6 Le génome de COVID ‐ 19 est un ARN à sens positif simple brin.7 L'analyse de séquence a montré que le COVID ‐ 19 possédait une structure génomique typique de coronavirus et appartenait au groupe de β ‐ coronavirus, y compris le SARS ‐ CoV et le MERS ‐ CoV.7 COVID ‐ 19 était à plus de 82% identique à ceux du SARS ‐ CoV.8, 9 COVID ‐ 19 pourrait se propager dans le monde entier avec la pandémie. Actuellement, il n'existe aucun traitement ni vaccin enregistré pour la maladie. En l'absence d'un traitement spécifique pour ce nouveau virus, il est urgent de trouver une solution alternative pour prévenir et contrôler la réplication et la propagation du virus. Nous avons effectué une recherche en ligne sur PubMed et Web of Science avec les mots clés SRAS, MERS et coronavirus. Nous résumons et proposons des options thérapeutiques disponibles pour le traitement de ces nouveaux coronavirus.
2 TRAITEMENT GÉNÉRAL DE L'INFECTION VIRALE
2.1 Interventions nutritionnelles
2.1.1 Vitamine A
La vitamine A est la première vitamine liposoluble à être reconnue et le β-carotène est son précurseur d'origine végétale (tableau 1). Il existe trois formes actives de vitamine A dans le corps, le rétinol, la rétine et l'acide rétinoïque. La vitamine A est également appelée vitamine «anti-infectieuse» et de nombreuses défenses de l'organisme contre l'infection dépendent d'un approvisionnement adéquat. Les chercheurs pensent qu'une altération de la réponse immunitaire est due à la carence d'un élément nutritionnel particulier.10 La carence en vitamine A est fortement impliquée dans la rougeole et la diarrhée11 et la rougeole peut devenir grave chez les enfants déficients en vitamine A. En outre, Semba et al12 ont signalé que la supplémentation en vitamine A réduisait la morbidité et la mortalité dans différentes maladies infectieuses, telles que la rougeole, les maladies diarrhéiques, la pneumonie liée à la rougeole, l'infection par le virus de l'immunodéficience humaine (VIH) et le paludisme. La supplémentation en vitamine A offre également une certaine protection contre les complications d'autres infections potentiellement mortelles, notamment le paludisme, les maladies pulmonaires et le VIH.13 Jee et al14 avaient signalé que les régimes pauvres en vitamine A pouvaient compromettre l'efficacité des vaccins inactivés contre les coronavirus bovins et rendre les veaux plus sensible aux maladies infectieuses. L'effet de l'infection par le virus de la bronchite infectieuse (IBV), une sorte de coronavirus, était plus prononcé chez les poulets nourris avec une alimentation légèrement déficiente en vitamine A que chez ceux nourris avec une alimentation adéquate en vitamine A.15 Le mécanisme par lequel la vitamine A et les rétinoïdes inhiber la réplication de la rougeole consiste à réguler positivement les éléments de la réponse immunitaire innée dans les cellules de spectateurs non infectées, ce qui les rend réfractaires à l'infection productive lors des cycles ultérieurs de réplication virale.16 Par conséquent, la vitamine A pourrait être une option prometteuse pour le traitement de ce nouveau coronavirus et la prévention de Infection pulmonaire.
Tableau 1. Traitements généraux de soutien
Options ciblées par virus et fonctions liées
2.1. Interventions nutritionnelles
2.1.1. Virus de la rougeole de la vitamine A, virus de l'immunodéficience humaine, coronavirus aviaire
2.1.2. Vitamines B MERS ‐ CoV; lésion pulmonaire induite par un ventilateur
2.1.3. Coronavirus aviaire à la vitamine C; infections des voies respiratoires inférieures
2.1.4. Coronavirus de la vitamine D bovine
2.1.5. Vitamine E Coxsackievirus, coronavirus bovin
2.1.6. Acides gras polyinsaturés oméga ‐ 3 (AGPI) Virus de la grippe, virus de l'immunodéficience humaine
2.1.7. Virus de la sélénium-grippe, coronavirus aviaire; mutations virales
2.1.8. Virus de la rougeole au zinc, SRAS-CoV
2.1.9. Mutations virales en fer
2.2. Immunoenhancers
2.2.1. Interférons SARS ‐ CoV, MERS ‐ CoV
2.2.2. Gammaglobuline intraveineuse SRAS ‐ CoV
2.2.3. Thymosine α ‐ 1 Augmente la résistance à la mort des thymocytes induite par les glucocorticoïdes
2.2.4. Thymopentine Restaurer la production d'anticorps
2.2.5. Lévamisole Agent immunostimulant ou agent immunosuppresseur
2.2.6. Cyclosporine A SARS ‐ CoV, virus de la bronchite infectieuse aviaire
2.2.7. Médecine chinoise SARS ‐ CoV, virus de la bronchite infectieuse aviaire
Abréviations: MERS-CoV, coronavirus du syndrome respiratoire du Moyen-Orient; SRAS-CoV, coronavirus du syndrome respiratoire aigu sévère.
2.1.2 Vitamines B
Les vitamines B sont des vitamines hydrosolubles et fonctionnent dans le cadre des coenzymes. Chaque vitamine B a ses fonctions spéciales. Par exemple, la vitamine B2 (riboflavine) joue un rôle dans le métabolisme énergétique de toutes les cellules. On soupçonnait une carence en vitamine B2 chez les personnes âgées aux États-Unis.17 Keil et al18 avaient rapporté que la vitamine B2 et la lumière UV réduisaient efficacement le titre de MERS-CoV dans les produits plasmatiques humains. La vitamine B3, également appelée nicotinamide, pourrait améliorer la destruction de Staphylococcus aureus grâce à un facteur de transcription spécifique aux myéloïdes et la vitamine B3 était efficace à la fois dans des contextes prophylactiques et thérapeutiques.19 - effet inflammatoire lors d'une lésion pulmonaire induite par le ventilateur. Cependant, elle a également conduit paradoxalement au développement d'une hypoxémie importante.20 La vitamine B6 est également nécessaire dans le métabolisme des protéines et elle participe à plus de 100 réactions dans les tissus corporels. En outre, il joue également un rôle important dans la fonction immunitaire du corps. Étant donné que la pénurie de vitamines B peut affaiblir la réponse immunitaire de l'hôte, elles doivent être administrées aux patients infectés par le virus pour renforcer leur système immunitaire. Par conséquent, les vitamines B pourraient être choisies comme option de base pour le traitement de COVID ‐ 19.
2.1.3 Vitamine C
La vitamine C est une autre vitamine hydrosoluble et elle est également appelée acide ascorbique, ce qui signifie «acide sans scorbut». La vitamine C est surtout connue pour son rôle dans la synthèse du collagène dans les tissus conjonctifs et agit comme antioxydant. La vitamine C soutient également les fonctions immunitaires et protège contre l'infection causée par un coronavirus.21 Par exemple, Atherton et al22 ont signalé que la vitamine C augmentait la résistance des cultures d'organes trachéaux d'embryons de poulet à l'infection par le coronavirus aviaire. La vitamine C peut également fonctionner comme un agent antihistaminique faible pour soulager les symptômes pseudo-grippaux tels que les éternuements, le nez qui coule ou bouché et les sinus enflés23. ‐Supplémented groupes, suggérant que la vitamine C pourrait prévenir la sensibilité aux infections des voies respiratoires inférieures dans certaines conditions.24 Le COVID ‐ 19 avait été signalé comme provoquant une infection des voies respiratoires inférieures, de sorte que la vitamine C pourrait être l'un des choix efficaces pour le traitement des COVID19.
2.1.4 Vitamine D
La vitamine D n'est pas seulement un nutriment mais aussi une hormone, qui peut être synthétisée dans notre corps à l'aide de la lumière du soleil. En plus de son rôle dans le maintien de l'intégrité osseuse, il stimule également la maturation de nombreuses cellules dont les cellules immunitaires. Un nombre élevé d'adultes en bonne santé auraient de faibles niveaux de vitamine D, principalement à la fin de la saison d'hiver.25 De plus, les personnes confinées à la maison ou en institution et celles qui travaillent la nuit peuvent avoir une carence en vitamine D, de même que de nombreuses personnes âgées, qui ont une exposition limitée au soleil.26 Le COVID ‐ 19 a été identifié pour la première fois à l'hiver 2019 et touchait principalement les personnes d'âge moyen à âgées. Les personnes infectées par le virus pourraient ne pas avoir suffisamment de vitamine D.En outre, la diminution du statut en vitamine D chez les veaux aurait provoqué l'infection du coronavirus bovin27. Par conséquent, la vitamine D pourrait fonctionner comme une autre option thérapeutique pour le traitement de ce nouveau virus. .
2.1.5 Vitamine E
La vitamine E est une vitamine liposoluble et comprend à la fois des tocophérols et des tocotriénols. La vitamine E joue un rôle important dans la réduction du stress oxydatif en se liant aux radicaux libres en tant qu'antioxydant.28 Une carence en vitamine E aurait intensifié les lésions myocardiques de l'infection par le coxsackievirus B3 (une sorte de virus à ARN) chez la souris29 et augmenté la virulence du coxsackievirus B3 chez la souris en raison d'une carence en vitamine E ou en sélénium.30 De plus, la diminution du statut en vitamine E et D chez les veaux a également provoqué l'infection du coronavirus bovin27.
2.1.6 Acides gras polyinsaturés oméga ‐ 3
Les acides gras polyinsaturés à longue chaîne (AGPI) sont d'importants médiateurs de l'inflammation et des réponses immunitaires adaptatives.31 Les AGPI oméga-3 et oméga-6 favorisent principalement les effets anti-inflammatoires et pro-inflammatoires. Ce sont des précurseurs de résolvines / protectines et de prostaglandines / leucotriènes, respectivement.31 Begin et al32 avaient étudié les taux de lipides plasmatiques chez les patients atteints du sida et avaient constaté un manque sélectif et spécifique des AGPI à longue chaîne des oméga-3, qui sont trouvé en fortes concentrations dans les huiles de poisson. De plus, la protectine D1, le médiateur lipidique dérivé des oméga-3 PUFA, pourrait considérablement atténuer la réplication du virus de la grippe via le mécanisme d'exportation d'ARN. De plus, le traitement de la protectine D1 avec du péramivir pourrait complètement sauver les souris de la mortalité due à la grippe.33 Leu et al34 avaient constaté que plusieurs AGPI avaient également des activités de lutte contre le virus de l'hépatite C (VHC). Par conséquent, les oméga ‐ 3, y compris la protectine D1, qui a servi de nouveau médicament antiviral, pourraient être envisagés pour l'une des interventions potentielles de ce nouveau virus, COVID ‐ 19.
2.1.7 Sélénium
Le sélénium est un oligo-élément essentiel pour la biologie redox des mammifères35. L'état nutritionnel de l'hôte joue un rôle très important dans la défense contre les maladies infectieuses.36 La carence nutritionnelle a un impact non seulement sur la réponse immunitaire mais aussi sur le pathogène viral lui-même.10 Carence alimentaire en sélénium qui provoque un stress oxydatif chez l'hôte peut altérer un génome viral de sorte qu'un virus normalement bénin ou légèrement pathogène peut devenir très virulent chez l'hôte déficient sous stress oxydatif.10 Une carence en sélénium induit non seulement une altération du système immunitaire de l'hôte, mais aussi une rapide la mutation de variantes bénignes des virus à ARN en virulence37. Beck et al38 avaient rapporté que la carence en sélénium pouvait non seulement augmenter la pathologie d'une infection par le virus de la grippe, mais aussi entraîner des changements dans le génome du coxsackievirus, permettant à un virus avirulent d'acquérir la virulence due à une mutation génétique. .39 C'est parce que le sélénium pourrait aider un groupe d'enzymes qui, de concert avec la vitamine E, agissent pour prévenir la formation de radicaux libres et prévenir les dommages oxydatifs aux cellules et aux tissus.37 Il a été signalé que l'effet synergique du sélénium avec les saponines de tige-feuille de ginseng pourrait induire une réponse immunitaire à un vaccin bivalent vivant contre la bronchite infectieuse contre le coronavirus chez les poulets.40 Par conséquent, le sélénium la supplémentation pourrait être un choix efficace pour le traitement de ce nouveau virus de COVID ‐ 19.
2.1.8 Zinc
Le zinc est un oligo-élément alimentaire et est important pour le maintien et le développement des cellules immunitaires du système immunitaire inné et adaptatif.41 Une carence en zinc entraîne un dysfonctionnement de l'immunité humorale et à médiation cellulaire et augmente la sensibilité aux maladies infectieuses.42 Supplément de zinc donné aux enfants carencés en zinc pourrait réduire la morbidité et la mortalité liées à la rougeole causées par les infections des voies respiratoires inférieures.43 L'augmentation de la concentration de zinc intracellulaire avec des zinc-ionophores comme la pyrithione peut efficacement entraver la réplication d'une variété de virus à ARN44. la combinaison de zinc et de pyrithione à de faibles concentrations inhibe la réplication du coronavirus du SRAS (SARS-CoV) .44 Par conséquent, le supplément de zinc peut avoir un effet non seulement sur les symptômes liés au COVID-19 comme la diarrhée et les infections des voies respiratoires inférieures, mais également sur le COVID -19 lui-même.
2.1.9 Fer
Le fer est nécessaire à la fois pour l'hôte et l'agent pathogène et une carence en fer peut altérer l'immunité de l'hôte, tandis qu'une surcharge en fer peut provoquer un stress oxydatif qui propage des mutations virales nocives.45 La carence en fer a été signalée comme un facteur de risque de développement d'infections aiguës récurrentes des voies respiratoires46
2.2 Immuno-agresseurs
2.2.1 Interférons
Les interférons (IFN) se sont divisés en interférons de type I et de type II. En tant que membre de l'IFN de type I, l'IFN ‐ α est produit très rapidement dans le cadre de la réponse immunitaire innée à l'infection par le virus. L'IFN ‐ α inhibe la réplication des coronavirus animaux et humains.47, 48 L'enquête in vitro a également démontré que les interférons de type I, y compris l'IFN ‐ β, pouvaient inhiber la réplication du SRAS ‐ CoV.49 Cependant, il a été signalé que l'interféron ‐ γ ne possédait pas d'antiviral activité contre le coronavirus du SRAS.50 Kuri et al51 ont en outre signalé que la transcription de l'IFN était bloquée dans les cellules tissulaires infectées par le SRAS-CoV et que les cellules étaient en mesure de restaurer partiellement leur réponse immunitaire innée au SRAS-CoV après un amorçage avec de petites quantités d'IFN. De plus, Tan et al avaient testé l'inhibition de l'infection par le coronavirus du SRAS in vitro avec des médicaments antiviraux cliniquement approuvés. Ils ont constaté que l'inhibition complète des effets cytopathiques du virus a été observée avec des sous-types spécifiques (β ‐ 1b, α ‐ n1, α ‐ n3 et interféron α des leucocytes humains) en culture.52 Haagmans et al54 ont également rapporté in vivo que des recombinants pégylés recombinants L'IFN ‐ α2b, un médicament homologué contre l'hépatite C chronique 53, pourrait protéger les pneumocytes de type 1 contre l'infection par le coronavirus du SRAS chez les singes (macaques). Le médicament administré 3 jours avant l'infection pourrait réduire la réplication virale et les lésions pulmonaires par rapport aux singes témoins55. Il était également considéré comme un médicament candidat pour le traitement du SRAS à cette époque et l'efficacité de l'IFN ‐ α recombinant synthétique pour le traitement des Des patients atteints du SRAS ont été démontrés dans un essai clinique pilote.56 De plus, les interférons se sont également révélés être de puissants inhibiteurs de la réplication du MERS-CoV.57 De plus, la combinaison d'interféron-α-2a et de ribavirine a été administrée à des patients atteints d'un MERS sévère. L'infection au CoV et la survie de ces patients ont été améliorées57. Ces résultats suggèrent que ces IFN approuvés pourraient également être utilisés pour le traitement de ce nouveau coronavirus.
2.2.2 Gammaglobuline intraveineuse
La gammaglobuline intraveineuse (IgIV) a été développée pour la première fois à la fin des années 1970 58 et est probablement le médicament immunomodulateur le plus sûr disponible pour une utilisation à long terme à tous les âges. Cependant, il a des effets indésirables. Lors de l'épidémie de SRAS en 2003, les IgIV ont été largement utilisés à Singapour. Cependant, un tiers des patients gravement malades ont développé une thromboembolie veineuse, y compris une embolie pulmonaire malgré l'utilisation d'héparine prophylactique de faible poids moléculaire.59 Cela était dû à l'augmentation de la viscosité induite par les IgIV dans les états hypercoagulables des patients atteints du SRAS.60
2.2.3 Thymosine α ‐ 1
La thymosine α ‐ 1 (Ta1) est une hormone peptidique thymique et elle a une capacité particulière à restaurer l'homéostasie du système immunitaire.61 Elle a été isolée pour la première fois du tissu thymique au milieu des années 60 et elle avait attiré beaucoup d'attention pour son immunostimulation Elle a été synthétisée chimiquement et utilisée dans des maladies où le système immunitaire était entravé ou altéré.63 Outre son rôle dans le développement des thymocytes, la thymosine α ‐ 1 pourrait également augmenter la résistance du thymocyte à la mort du thymocyte.64 pourrait également être utilisé comme activateur immunitaire pour les patients atteints du SRAS et il était efficace pour contrôler la propagation de la maladie.65, 66 La méthylprednisolone était souvent utilisée pendant le traitement actuel de COVID-19 et l'effet secondaire de la mort des thymocytes induite par les corticoïdes devrait être pris en considération. Il est donc sage d'utiliser la thymosine α1 avant l'administration de méthylprednisolone.
2.2.4 Thymopentine
Il a été démontré que la thymopentine (TP5, munox), un pentapeptide synthétique correspondant au site actif de la thymopoïétine, rétablit la production d'anticorps chez les souris âgées.67 De plus, elle pourrait améliorer la réponse en anticorps chez l'homme lorsqu'elle est appliquée par voie sous-cutanée trois fois par semaine à des doses de 50 mg.68 De plus, la thymopentine pourrait également être utilisée comme traitement adjuvant pour les non-répondeurs ou les hyporépondeurs à la vaccination contre l'hépatite B.69
2.2.5 Lévamisole
Le lévamisole, un composé synthétique de faible poids moléculaire, est le premier membre d'une nouvelle classe de médicaments qui peuvent augmenter les fonctions de l'immunité cellulaire chez des animaux de laboratoire normaux et sains70. Cependant, le lévamisole peut agir soit comme un agent immunostimulant soit agent en fonction du dosage et du moment. Ainsi, son utilisation clinique doit être soigneusement prise. Joffe et al71 avaient rapporté que le traitement au lévamisole et à l'acide ascorbique in vitro pouvait inverser la sous-population déprimée d'aide / inducteur des lymphocytes dans la rougeole. Par conséquent, l'utilisation du lévamisole pourrait également être envisagée pour le traitement du COVID ‐ 19.
2.2.6 Cyclosporine A
La cyclosporine A est un médicament immunosuppresseur très important et elle a été largement utilisée en transplantation. L'utilisation émergente de la cyclosporine A a considérablement amélioré les taux de survie des patients et des greffons après une transplantation d'organe solide.72 La cyclosporine A est également utilisée pour le traitement des troubles auto-immunes. Luo et al73 avaient émis l'hypothèse que la protéine nucléocapside (NP) du SRAS-CoV jouait un rôle important dans le processus d'assemblage et de libération des particules virales et qu'elle pourrait également se lier à la cyclophiline A. La cyclophiline A est un membre clé des immunophilines agissant comme un cellulaire récepteur de la cyclosporine A.74 La cyclophiline A a joué un rôle important dans l'infection virale qui facilite ou inhibe leur réplication74. En outre, l'inhibition des cyclophilines par la cyclosporine A pourrait bloquer la réplication des coronavirus de tous les genres, y compris le SRAS-CoV comme ainsi que le virus de la bronchite infectieuse aviaire.75 Par conséquent, les dérivés non immunosuppresseurs de la cyclosporine A pourraient servir d'inhibiteurs de coronavirus à large spectre applicables contre le nouveau COVID ‐ 19 émergent de type viral.
2.2.7 Médecine chinoise
La glycyrrhizine est un composant actif des racines de réglisse dans la médecine chinoise. Cinatl et al76 avaient rapporté que la glycyrrhizine pouvait inhiber la réplication du virus associé au SRAS in vitro et elle avait déjà été suggérée comme une option alternative pour le traitement du SRAS à l'époque. Le baicalin, une autre plante chinoise, est un flavonoïde isolé de Radix Scutellaria. La baicaline s'est également révélée capable d'inhiber le SRAS-CoV in vitro.50 Les saponines de tiges de feuilles de ginseng pourraient grandement améliorer les réponses spécifiques en anticorps contre le virus de la maladie de Newcastle et le virus de la bronchite infectieuse.40 Par conséquent, la médecine chinoise pourrait également être considérée comme choix d'améliorer l'immunité de l'hôte contre l'infection par COVID ‐ 19.
En résumé, le traitement général de l'infection virale, y compris les interventions nutritionnelles et toutes sortes d'immuno-agresseurs, a été utilisé pour renforcer l'immunité de l'hôte contre les infections virales à ARN. Par conséquent, ils peuvent également être utilisés pour lutter contre l'infection au COVID ‐ 19 en corrigeant la lymphopénie des patients.
3 TRAITEMENTS SPÉCIFIQUES AUX CORONAVIRUS
3.1 Inhibiteurs de la protéase coronavirale
La chymotrypsine (3C) et la papaïne (PLP) sont des protéines codées par le coronavirus (tableau 2). Ils ont une fonction essentielle pour la réplication coronavirale et ont également une fonction supplémentaire pour l'inhibition des réponses immunitaires innées de l'hôte. Le ciblage de la protéase de type 3C (3 CLpro) et de la protéase de type papaïne (PLpro) est plus attrayant pour le traitement du coronavirus.77
Tableau 2. Traitements spécifiques aux coronavirus
3.1. Inhibiteurs de la protéase du coronavirus
3.1.1. Inhibiteurs de type chymotrypsine (de type 3C)
3.1.1.1. Cinanserin
3.1.1.2. Flavonoïdes
3.1.2. Inhibiteurs de la protéase papuleuse (PLP)
3.1.2.1. Diarylheptanoïdes
3.2. Bloqueurs de l'enzyme 2 de conversion de l'angiotensine (ACE2) protéique Spike (S)
3.2.1. Anticorps monoclonal humain (mAb)
3.2.2. Chloroquine
3.2.3. Emodin
3.2.4. Promazine
3.2.5. Nicotianamine
3.1.1 Inhibiteurs de type chymotrypsine (de type 3C)
Cinanserin
La cinansérine, un ancien médicament, est bien connue pour son antagoniste des récepteurs de la sérotonine. Il pourrait inhiber la 3 protéase de type chymotrypsine (3C) et était un inhibiteur prometteur de la réplication du SRAS-CoV.78 Le 3CLpro s'est également avéré être codé dans COVID-19.7 Par conséquent, la cinansérine peut être un meilleur choix pour le traitement de l'infection par COVID ‐ 19.
Flavonoïdes
Les flavonoïdes sont une classe importante de produits naturels et ont plusieurs sous-groupes, qui comprennent les chalcones, les flavones, les flavonols et les isoflavones.79 Les flavonoïdes ont de nombreuses fonctions en plus des effets antioxydants et ils ont également des capacités antivirales. Shimizu et al80 avaient découvert que les flavonoïdes de Pterogyne Nitens pouvaient inhiber l'entrée du virus de l'hépatite C. Jo et al81 avaient suggéré que l'activité anti-coronavirus de certains flavonoïdes (Herbacétine, rhoifoline et pectolinarine) était due à l'inhibition de la protéase de type 3C (3CLpro). D'autres flavonoïdes (l'herbacétine, l'isobavachalcone, la quercétine 3 ‐ β ‐ d ‐ glucoside et l'hélichrysetine) se sont également révélés capables de bloquer l'activité enzymatique du MERS ‐ CoV / 3CLpro.82 En outre, Ryu et al83 ont signalé que des biflavonoïdes de Torreya nucifera a également apporté un effet inhibiteur du SARS-CoV / 3CL (pro).
3.1.2 Inhibiteurs de protéase de type papaïne
La protéase de type papaïne (PLP) du coronavirus humain est une nouvelle deubiquitinase codée virale et est un antagoniste de l'IFN pour l'inhibition de la réponse immunitaire antivirale innée de l'hôte.
Diarylheptanoïdes
Les diarylheptanoïdes sont un produit naturel et sont extraits de l'écorce de tige d'Alnus japonica. Il s'est avéré être capable d'inhiber la protéase de type papaïne du SRAS-CoV.77
Par conséquent, la cinansérine ainsi que les flavonoïdes et d'autres composés naturels pourraient être choisis comme choix alternatifs pour lutter contre l'infection au COVID ‐ 19 en ciblant les protéases coronavirales.
3.2 Bloqueurs de l'enzyme 2 de conversion de l'angiotensine (ACE2) protéique Spike (S)
L'enzyme 2 de conversion de l'angiotensine (ACE2) est une protéine membranaire intégrale de type I qui fonctionne comme une carboxypeptidase et est le premier homologue humain de l'ACE.84 ACE2 hydrolyse efficacement le puissant vasoconstricteur angiotensine II en angiotensine (1‐7) et elle a été impliqué dans l'hypertension, la fonction cardiaque, la fonction cardiaque et le diabète.84 De plus, l'ACE2 est également un récepteur fonctionnel du SRAS-CoV et il assure la médiation de l'entrée du virus dans la cellule en se liant à la protéine spike (S) 85, 86 La protéine S du SRAS-CoV est une glycoprotéine de surface de type I et est responsable de la liaison aux récepteurs cellulaires. De plus, la protéine S intervient dans la fusion des membranes virales et hôtes.87 Zhou et al ont rapporté que COVID ‐ 19 a utilisé l'ACE2 comme seul récepteur pour l'entrée, mais n'a pas utilisé d'autres récepteurs de coronavirus, l'aminopeptidase N et la dipeptidyl peptidase, pour l'entrée . Le blocage de la liaison de la protéine S à l'ACE2 est important pour le traitement de l'infection par le SRAS-CoV.88
3.2.1 Anticorps monoclonal humain
Sui et al avaient trouvé un anticorps monoclonal humain recombinant (mAb) (fragments de région variable à chaîne unique, scFvs 80R) contre le domaine S1 de la protéine S du SARS-CoV à partir de deux bibliothèques d'anticorps humains non immuns. Le mAb pourrait neutraliser efficacement le SRAS-CoV et inhiber la formation de syncyties entre les cellules exprimant la protéine S et celles exprimant le récepteur du SARS-CoV ACE2.89
3.2.2 Chloroquine
La chloroquine est une 9-aminoquinoléine connue depuis 1934. Outre ses effets antipaludiques bien connus, le médicament possède également de nombreuses propriétés biochimiques intéressantes, notamment un effet antiviral. De plus, il avait été utilisé contre l'infection virale.90 De plus, la chloroquine s'est également révélée être un puissant inhibiteur de l'infection par le coronavirus du SRAS en interférant avec l'ACE2, l'un des sites de liaison de la surface cellulaire pour la protéine S du SARS-CoV.91
3.2.3 Emodin
L'émodine est un composé anthraquinone dérivé du genre Rheum et Polygonum et c'est également un agent virucide.92 L'émodine pourrait bloquer de manière significative l'interaction entre la protéine S du SRAS-CoV et l'ACE2. Par conséquent, l'émodine pourrait abolir l'infection par le SRAS-CoV en rivalisant pour le site de liaison de la protéine S avec l'ACE2.93
3.2.4 Promazine
La promazine, médicament antipsychotique, partage une structure similaire avec l'émodine. Il a été démontré qu'il présente un effet significatif sur l'inhibition de la réplication du SRAS-CoV.94 Par rapport à l'émodine, la promazine a montré une puissante inhibition de la liaison de la protéine S à l'ACE2. Ces résultats suggèrent que l'émodine et la promazine pourraient être en mesure d'inhiber l'infectiosité du SRAS-CoV en bloquant l'interaction de la protéine S et de l'ACE2.93 Par conséquent, l'anticorps monoclonal (scFv80R), la chloroquine, l'émodine et la promazine pourraient être utilisés comme choix alternatifs pour le traitement de COVID ‐ 19.
3.2.5 Nicotianamine
La nicotianamine est un ligand métallique important dans les plantes95 et on trouve un nouvel inhibiteur de l'enzyme ‐ 2 convertissant l'angiotensine dans le soja.96 C'est donc une autre option potentielle à utiliser pour réduire l'infection au COVID ‐ 19.
4 TRAITEMENTS ANTIVIRAUX
4.1 Ribavirine
La ribavirine, un agent antiviral à large spectre, est couramment utilisée pour traiter l'hépatite C (tableau 3). Au cours de l'épidémie de SRAS, la ribavirine a été largement utilisée dans la plupart des cas avec ou sans utilisation concomitante de stéroïdes à Hong Kong.97 Cependant, il y avait un scepticisme considérable de la part d'experts étrangers et locaux sur l'efficacité de la ribavirine.98 Parce qu'un rapport mentionnait que la ribavirine n'a eu aucune activité significative contre le SRAS-CoV in vitro52 et l'utilisation de la ribavirine s'est avérée être associée à une toxicité significative, y compris l'hémolyse (dans 76%) et une diminution de l'hémoglobine (dans 49%) .99 Cependant, Morgenstern et al49 ont rapporté que la ribavirine et l'interféron-β inhibaient en synergie la réplication du coronavirus associé au SRAS dans les lignées cellulaires animales et humaines. Compte tenu des effets indésirables et du manque d'efficacité in vitro, l'utilisation de la ribavirine doit être sérieusement envisagée pour le traitement de COVID ‐ 19, même en association avec d'autres médicaments antiviraux.
capable 3. Traitements antiviraux et autres composés
4. Traitements antiviraux
4.1. Ribavirine
4.2. Lopinavir (LPV) / ritonavir (RTV) (Kaletra)
4.3. Remdesivir
4.4. Nelfinavir
4.5 Arbidol
4.6. L'oxyde nitrique
5. Autres composés
5.1. Acide α ‐ lipoïque
5.2. Estradiol et phytoestrogène
5.3. Mucroporine ‐ M1
4.2 Lopinavir / ritonavir (kaletra)
La combinaison du lopinavir avec le ritonavir est largement utilisée comme inhibiteur de protéase boosté dans le traitement de l'infection par le VIH.100 Le lopinavir (LPV) est généralement associé au ritonavir (RTV) pour augmenter la demi-vie du lopinavir par l'inhibition du cytochrome P450.101 Chu et al102 avait constaté que l'utilisation du LPV / RTV avec la ribavirine dans le traitement du SRAS était associée à de meilleurs résultats. Kim et al103 avaient également signalé un cas réussi de maladie MERS-CoV traitée par une triple thérapie LPV / RTV, la ribavirine et l'IFN-α2a en Corée du Sud. En ce qui concerne ce nouveau virus, COVID-19, la triple thérapie de Kim devrait être considérée comme une option au stade précoce de la maladie.
4.3 Remdesivir
Le remdesivir (RDV), un analogue nucléosidique GS ‐ 5734, aurait inhibé le coronavirus humain et zoonotique in vitro et freiné le coronavirus du syndrome respiratoire aigu sévère (SRAS ‐ CoV) in vivo.104 Récemment, l'activité antivirale du RDV et de l'IFN‐ Le β s'est révélé supérieur à celui du LPV / RTV ‐ IFN ‐ β contre le MERS ‐ CoV in vitro et in vivo.101 De plus, le RDV pourrait améliorer la fonction pulmonaire et réduire la charge virale pulmonaire et la pathologie pulmonaire sévère chez la souris, ce qui était impossible pour LPV / RTV ‐ IFN ‐ β.101 Récemment, un premier cas infecté par COVID ‐ 19 a été signalé aux États-Unis et l'utilisation de remdesivir a été administrée lorsque l'état clinique du patient empirait.105 Par conséquent, l'utilisation de RDV avec L'IFN ‐ β pourrait être un meilleur choix pour le traitement du COVID ‐ 19 par rapport à celui de la triple combinaison LPV / RTV ‐ IFN ‐ β. Cependant, des essais randomisés et contrôlés sont encore nécessaires pour déterminer l'innocuité et l'efficacité du remdesivir.
4.4 Nelfinavir
Le nelfinavir est un inhibiteur sélectif de la protéase du VIH, qui est responsable du traitement post-traductionnel des propeptides du VIH.106 Yamamoto et al107 avaient découvert que le nelfinavir pouvait fortement inhiber la réplication du SRAS-CoV. Par conséquent, le nelfinavir pourrait également être une option pour le traitement du COVID ‐ 19.
4.5 Arbidol
Arbidol (ARB) est une petite molécule dérivée d'indole de fabrication russe et est autorisée en Russie et en Chine pour la prophylaxie et le traitement de la grippe et d'autres infections virales respiratoires.108 Il a été constaté qu'Arbidol était capable de bloquer la fusion virale contre la grippe A et B ainsi que le virus de l'hépatite C.109 Arbidol pourrait également inhiber le virus de l'hépatite C en bloquant l'entrée et la réplication du virus de l'hépatite C in vitro.110 En outre, l'arbidol et ses dérivés, le mésylate d'arbidol, auraient une activité antivirale contre le pathogène de Le SRAS dans les cultures cellulaires et le mésylate d'arbidol était presque 5 fois plus efficace que l'arbidol pour réduire la reproduction du virus du SRAS dans les cellules en culture.111
4.6 Oxyde nitrique
L'oxyde nitrique (NO) est un gaz aux activités biologiques diverses et est produit à partir de l'arginine par les NO synthases. Le NO est capable d'interagir avec le superoxyde, formant du peroxynitrite, qui, à son tour, peut médier des réactions bactéricides ou cytotoxiques.112 De plus, le NO a joué un rôle important dans la régulation de la fonction des voies aériennes et dans le traitement des maladies inflammatoires des voies aériennes.113 Rossaint et al114 ont rapporté que les effets bénéfiques de l'inhalation de NO ont pu être observés chez la plupart des patients atteints d'un syndrome de détresse respiratoire aiguë sévère. Le NO s'est également révélé inhiber la synthèse des protéines virales et de l'ARN.115 De plus, Akerström et al116 avaient rapporté que le donneur de NO organique, la S ‐ nitroso ‐ N ‐ acétylpénicillamine, pourrait inhiber de manière significative le cycle de réplication du SRAS ‐ CoV dans une concentration dépendante de la concentration manière. Par conséquent, l'inhalation de NO pourrait également être choisie comme option pour le traitement des patients gravement infectés par COVID ‐ 19.
5 AUTRES COMPOSÉS
5.1 Acide α ‐ lipoïque
L'acide α ‐ lipoïque (ALA), un composé disulfure naturel, agit comme une coenzyme cellulaire et est utilisé depuis des années pour le traitement des polyneuropathies et des troubles hépatiques (tableau 3) .117 L'ALA, en tant qu'antioxydant, a joué un rôle central dans la récupération des radicaux libres pour se protéger contre les dommages oxydatifs dans plusieurs maladies.118 En outre, l'ALA avait également sa capacité à augmenter les niveaux de glutathion intracellulaire (GSH) 118 et à normaliser le stress oxydatif induit par la dexaméthasone chez le poulet.119 Wu et al120 ont également indiqué que le le stress oxydatif dans les cellules hôtes était un facteur important dans l'infectiosité du coronavirus humain 229E et la carence en glucose ‐ 6 ‐ phosphate déshydrogénase (G6PD) était un autre facteur qui augmentait l'infection par le coronavirus humain 229E. L'ajout d'acide α-lipoïque aux cellules knock-down G6PD pourrait atténuer la sensibilité accrue à l'infection par le coronavirus 229E.120 Fait intéressant, Baur et al121 ont également constaté que l'acide α-lipoïque était efficace pour inhiber la réplication du VIH-1. En résumé, nous supposons que l'ALA pourrait également être utilisé comme thérapie facultative pour ce nouveau virus.
5.2 Estradiol et phytoestrogène
Les femmes, en général, développent des réponses immunitaires plus robustes aux défis viraux que les hommes, ce qui peut entraîner une clairance virale plus efficace.122 Des études épidémiologiques ont montré que les hommes connaissaient un taux d'incidence et de létalité plus élevé que les femmes après une infection par le SRAS-CoV.123, 124 Au cours de l'épidémie de MERS, le taux d'occurrence de la maladie chez les hommes était près de deux fois plus élevé que chez les femmes et le taux de létalité était le même que le taux d'occurrence chez les hommes et les femmes.125 En outre, Channappanavar et al ont signalé que des souris mâles étaient plus sensibles à l'infection par le SRAS-CoV que les souris femelles de même âge. Cependant, la mortalité a augmenté chez les souris femelles lorsque l'ovariectomie a été effectuée ou que l'antagoniste des récepteurs aux œstrogènes a été administré.126 Wei et al127 ont également constaté que les taux sériques de prolactine, d'hormone folliculo-stimulante et d'hormone lutéinisante des patients atteints du SRAS étaient significativement plus élevés que ceux des groupes témoins, tandis que l'estradiol (E2), l'hormone de grossesse et l'hormone stimulant la thyroïde étaient considérablement inférieurs à ceux des témoins normaux. Il est intéressant de noter que les composés œstrogéniques réduisaient la réplication du virus de la grippe A dans les cellules épithéliales nasales humaines primaires dérivées de donneurs féminins, mais non masculins.128 En outre, le resvératrol, un phytoestrogène provenant des pépins de raisin et du vin rouge, aurait été un un puissant agent anti ‐ MERS in vitro.129 Par conséquent, le 17β ‐ estradiol ou le phytoestrogène pourraient également être une option alternative à envisager pour le traitement du COVID ‐ 19.
5.3 Mucroporine ‐ M1
La mucroporine ‐ M1 est un peptide dérivé du venin de scorpion et possède une activité virucide à large spectre contre de nombreux virus, notamment la rougeole, les virus de la grippe H5N1 et le SRAS ‐ CoV.130 Par conséquent, ce peptide pourrait également être utilisé pour le traitement de l'infection au COVID ‐ 19 comme ainsi que la nouvelle conception du médicament pour cibler COVID ‐ 19.
6. CONCLUSION
Dans cette revue, nous résumons toutes les interventions potentielles pour l'infection au COVID ‐ 19 selon les traitements antérieurs du SRAS et du MERS. Nous avons constaté que les traitements généraux sont très importants pour améliorer la réponse immunitaire de l'hôte contre l'infection virale à ARN. Il a souvent été démontré que la réponse immunitaire était affaiblie par une nutrition inadéquate dans de nombreux systèmes modèles ainsi que dans des études sur l'homme. Cependant, l'état nutritionnel de l'hôte, jusqu'à récemment, n'a pas été considéré comme un facteur contribuant à l'émergence de maladies infectieuses virales. Par conséquent, nous proposons de vérifier l'état nutritionnel des patients infectés par COVID ‐ 19 avant l'administration de traitements généraux. De plus, nous avons également constaté que les traitements spécifiques aux coronavirus et les traitements antiviraux étaient très utiles pour le traitement du SRAS et du MERS. Ils doivent également être considérés comme des traitements potentiels de l'infection au COVID ‐ 19. Les autres composés doivent également être choisis comme options alternatives pour le traitement ainsi que de nouvelles conceptions de médicaments.
Pour achever l'éradication de l'infection virale, les vaccins liés au COVID ‐ 19 sont garantis. Le développement d'un vaccin contre le SRAS avait déjà attiré l'attention de nombreux scientifiques dans le passé. L'IBV aviaire est similaire au SARS-CoV et les deux virus appartiennent au coronavirus. IBV est dans le groupe 3 et le SRAS appartient au groupe 4.131 Bijlenga et al55 avaient suggéré que le vaccin contre le virus vivant aviaire IBV (souche H) soit utilisé pour traiter le SRAS en 2005. Cependant, des tests préliminaires chez le singe devraient être effectués avant le démarrage. Fait intéressant, les enfants sont rarement attaqués par le COVID ‐ 19 ainsi que le SRAS ‐ CoV. Cela peut être dû au programme de vaccination requis pour chaque enfant. Les vaccins à virus ARN et les adjuvants des programmes de vaccination peuvent aider les enfants à échapper à l'infection. Par conséquent, les vaccins liés au virus à ARN, y compris la rougeole (MeV), la polio, le virus de l'encéphalite japonaise, le virus de la grippe et les vaccins liés à la rage, pourraient être utilisés comme choix alternatifs les plus prometteurs pour prévenir la transmission interhumaine par la vaccination. soignants et population non infectée.
De nombreux chercheurs ont également essayé le vaccin recombinant contre la rougeole exprimant la protéine S du SRAS et du MERS. Escriou et al132 avaient généré des candidats vaccinaux recombinants atténués vivants exprimant la protéine S ancrée dans la membrane du SRAS-CoV (SARS-CoV-S-vaccin) et ils avaient découvert que le vaccin pouvait induire les titres les plus élevés d'anticorps neutralisants et d'animaux immunisés protégés du défi infectieux intranasal avec le SRAS-CoV. Bodmer et al133 avaient rapporté que deux vaccins vivants atténués contre le virus de la rougeole exprimant soit la protéine S soit la protéine N du MERS-CoV pouvaient induire des réponses cellulaires T robustes et multifonctionnelles dans le modèle murin. Frantz et al134 ont également mentionné que le vaccin recombinant contre la rougeole pourrait induire des réponses biaisées plus fortes et T helper 1.
En ce qui concerne la protection à court terme et la prévention des infections virales, l'immunothérapie passive ne doit pas être négligée.135 La thérapie par anticorps monoclonaux est l'une des meilleures formes d'immunothérapie passive. Un mAb IgG1 humain, CR3014, avait été généré et il s'était révélé réactif avec le coronavirus du SRAS inactivé entier. De plus, le CR3014 pourrait être utilisé comme prophylaxie de l'infection par le coronavirus du SRAS chez les furets.136 Cependant, le CR3014 s'est révélé capable de bloquer l'interaction dans la souche parentale du SRAS-CoV, mais pas dans les variantes d'échappement. Cela a conduit à l'inefficacité du CR3014 pour prévenir l'infection chez l'homme. Le CR3022 était un autre anticorps monoclonal et il avait été démontré qu'il neutralisait les virus d'échappement CR3014.136 La combinaison de CR3014 et CR3022 avait également été signalée comme ayant le potentiel de contrôler la fuite immunitaire.135 Cependant, l'essai clinique de CR3022 avec CR3014 n'avait jamais été tenté. en raison du coût élevé de fabrication.
Le plasma convalescent peut également être appelé immunothérapie passive. Il est généralement choisi lorsqu'il n'y a pas de vaccins ou de médicaments spécifiques disponibles pour les maladies émergentes liées à l'infection.137 Arabi et al ont testé la faisabilité de la thérapie plasmatique convalescente ainsi que sa sécurité et son efficacité clinique chez les patients atteints de MERS gravement malades. Ils ont constaté que le plasma de convalescence avait un potentiel immunothérapeutique pour le traitement de l'infection par le MERS-CoV.138 De plus, le plasma de convalescence des patients guéris du SRAS avait également été signalé comme étant utile cliniquement pour le traitement d'autres patients atteints du SRAS.139, 140 Il est important de noter que l'utilisation de le plasma ou le sérum convalescent a également été suggéré par l'Organisation mondiale de la santé dans le cadre du Réseau des régulateurs du sang lorsque les vaccins et les médicaments antiviraux n'étaient pas disponibles pour un virus émergent. En résumé, ces résultats suggèrent que les vaccins actuels pour enfants liés au virus de l'ARN sont les meilleures méthodes alternatives à utiliser pour vacciner les personnes non infectées et les agents de santé. Le plasma convalescent doit être utilisé systématiquement pour le traitement des patients gravement malades infectés par COVID ‐ 19 s'il est disponible. Le vaccin aviaire contre l'IBV est également un autre choix pour les essais cliniques si sa sécurité a été approuvée chez le singe. Par conséquent, nous suggérons que toutes les interventions potentielles soient mises en œuvre pour contrôler le COVID ‐ 19 émergent si l'infection est incontrôlable.