Traduction de l'étude
 L'administration orale d'acides aminés à chaîne ramifiée atténue l'athérosclérose en inhibant la réponse inflammatoire et en régulant le microbiote intestinal chez des souris déficientes en ApoE
L'administration orale d'acides aminés à chaîne ramifiée atténue l'athérosclérose en inhibant la réponse inflammatoire et en régulant le microbiote intestinal chez des souris déficientes en ApoEpar Ziyun Li Nutrients 2022, 14(23), 5065 ;
L'athérosclérose (SA) est une maladie inflammatoire chronique qui sert de fondement pathogène commun à diverses maladies cardiovasculaires. Bien que des niveaux élevés d'acides aminés à chaîne ramifiée circulants (BCAA) puissent représenter un facteur de risque pour la SA, il n'est pas clair si la supplémentation alimentaire en BCAA provoque des niveaux élevés de BCAA circulants et donc influence la SA, et les mécanismes associés ne sont pas bien compris. Ici, des souris déficientes en ApoE (ApoE-/-) ont été nourries avec un régime alimentaire complété avec ou sans BCAA pour étudier les effets des BCAA sur la SA et déterminer les mécanismes potentiels associés. Dans cette étude, par rapport au régime riche en graisses (HFD), un régime riche en graisses complété par des BCAA (HFB) a réduit la zone de lésion athéroscléreuse et a provoqué une diminution significative du cholestérol sérique (TC) et du cholestérol à lipoprotéines de basse densité (LDL- C) niveaux. La supplémentation en BCAA a supprimé la réponse inflammatoire systémique en réduisant l'infiltration des macrophages ; abaisser les taux sériques de facteurs inflammatoires, y compris la protéine chimioattractante des monocytes-1 (MCP-1), le facteur de nécrose tumorale-α (TNF-α), l'interleukine-1β (IL-1β) et l'interleukine-6 (IL-6); et la suppression des voies de signalisation liées à l'inflammation. De plus, la supplémentation en BCAA a modifié la diversité et la composition des bactéries intestinales bêta, en particulier en réduisant les bactéries nocives et en augmentant les bactéries probiotiques, ainsi qu'en augmentant l'excrétion des acides biliaires (BA). De plus, les niveaux d'AB totaux, d'AB primaires, d'acides biliaires 12α-hydroxylés (12α-OH BA) et d'acides biliaires non 12α-hydroxylés (non-12α-OH BA) dans le contenu cæcal et colique ont augmenté dans le groupe HFB. de souris par rapport au groupe HFD.
Dans l'ensemble, ces données indiquent que la supplémentation alimentaire en BCAA peut atténuer l'athérosclérose induite par HFD chez les souris ApoE-/- grâce à une amélioration de la dyslipidémie et de l'inflammation, des mécanismes impliquant le microbiote intestinal et de la promotion de l'excrétion de BA
.
Les acides aminés à chaîne ramifiée favorisent la réparation des dommages musculaires induits par l'exercice en améliorant la polarisation des macrophages
Front Yunfeng Dong. Physiol., 06 décembre 2022
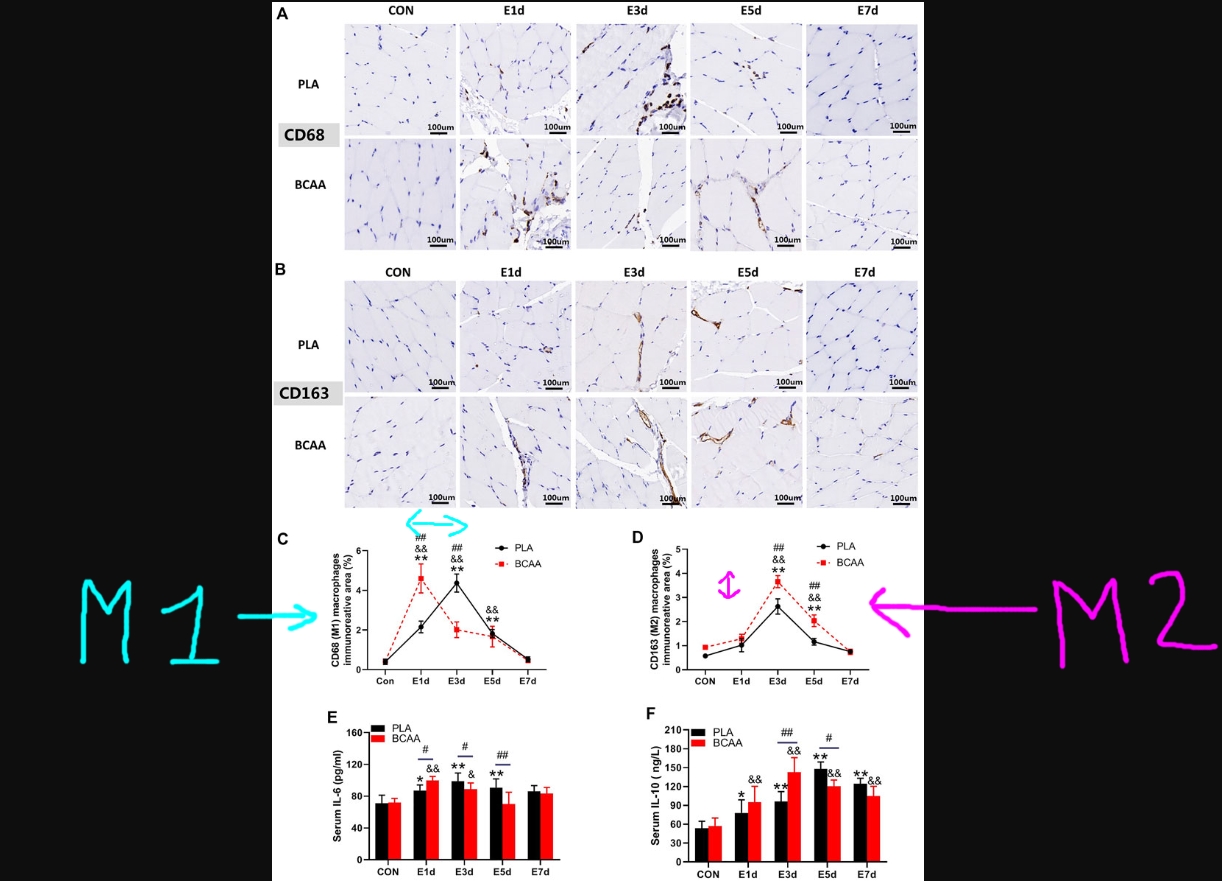
La réparation des dommages musculaires induits par l'exercice (EIMD) est étroitement liée à l'inflammation. Les acides aminés à chaîne ramifiée (BCAA), en tant que complément nutritionnel, favorisent la réparation des EIMD ; cependant, le mécanisme sous-jacent reste incertain. In vivo, des rats Sprague-Dawley ont été soumis à l'exercice excentrique d'Armstrong (une descente de 120 minutes avec une pente de -16° et une vitesse de 16 m min-1) pour induire l'EIMD et un supplément de BCAA a été administré par gavage oral. L'expression protéique des macrophages (CD68 et CD163) et des facteurs de régulation myogéniques (MYOD et MYOG) dans le gastrocnémien a été analysée. Les niveaux de cytokines inflammatoires et de créatine kinase (CK) dans le sérum ont également été mesurés. In vitro, des macrophages péritonéaux de souris ont été incubés avec du lipopolysaccharide (LPS) ou de l'IL-4 avec ou sans BCAA dans un milieu de culture. Pour l'expérience de co-culture, des cellules C2C12 ont été cultivées avec le milieu conditionné de macrophages préstimulés avec du LPS ou de l'IL-4 en présence ou en l'absence de BCAA.
L'étude actuelle a indiqué que la supplémentation en BCAA améliorait la polarisation M1/M2 des macrophages dans le muscle squelettique pendant la réparation EIMD, et que les BCAA favorisaient la polarisation M1 en améliorant la voie de glycolyse mTORC1-HIF1α et favorisaient la polarisation M2 indépendamment de mTORC1. De plus, les macrophages M1 promus par les BCAA ont stimulé davantage la prolifération des cellules satellites musculaires, tandis que les macrophages M2 promus par les BCAA ont stimulé leur différenciation.
Ensemble, ces résultats montrent que les macrophages médient les impacts bénéfiques des BCAA sur la réparation de l'EIMD en stimulant la prolifération et la différenciation des cellules satellites musculaires, mettant en lumière le rôle critique de l'inflammation dans la réparation de l'EIMD et les stratégies nutritionnelles potentielles pour améliorer les dommages musculaires.
Généralement, les macrophages se divisent en deux types
: les macrophages M1 activés de manière classique et les macrophages M2 activés alternativement. Les macrophages M1 sont présents dans la période pro-inflammatoire de l'EIMD et associés à la prolifération des SC (Otis et al., 2014 ; Varga et al., 2016), tandis que les macrophages M2 sont présents dans la période anti-inflammatoire de l'EIMD et associés aux SC. processus de différenciation et de réparation des tissus